Insulino-resistenza: una condizione metabolica che può interessare sia sedentari che sportivi
Molti pensano che l’insulino-resistenza sia semplicemente la conseguenza di “mangiare troppi zuccheri”. La realtà è molto più complessa: questo fenomeno metabolico può interessare sia persone sedentarie sia sportivi e dipende da diversi fattori legati allo stile di vita e al bilancio energetico. In questo articolo analizziamo cosa succede davvero nel metabolismo e quali strategie aiutano a preservare una buona sensibilità insulinica
Dott. Aaron Farina
3/7/20268 min read
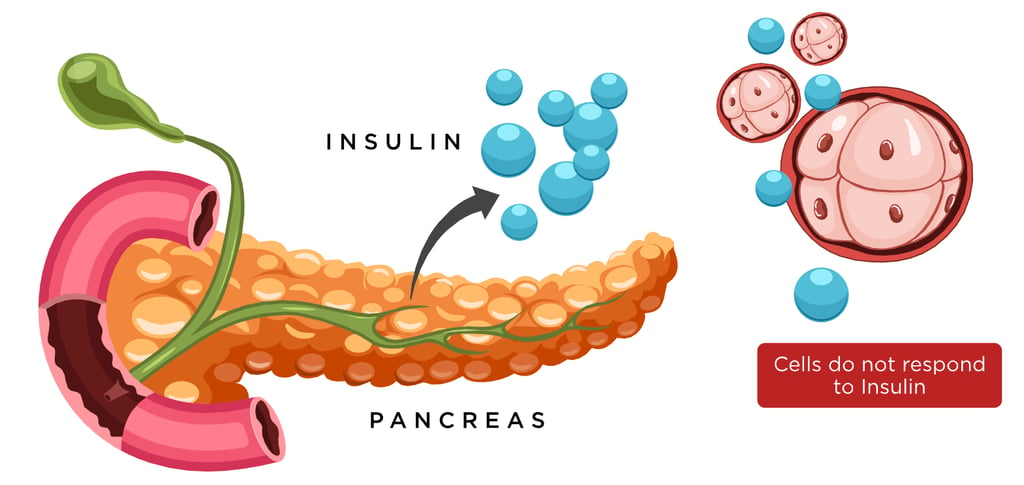
Cos’è l’insulino-resistenza
L’insulino-resistenza (IR) è una condizione metabolica in cui i tessuti periferici sensibili all’insulina, in particolare muscolo scheletrico e tessuto adiposo, mostrano una risposta ridotta all’azione dell’ormone. In termini pratici, a parità di concentrazione di insulina circolante, la capacità dell’organismo di favorire la captazione e l’utilizzo del glucosio risulta meno efficiente. Questo fenomeno rappresenta uno dei meccanismi centrali nello sviluppo di diverse condizioni metaboliche, tra cui il diabete di tipo 2 e la sindrome metabolica (Chadt & Al-Hasani, 2020; Zhao et al., 2023).
Come funziona normalmente l’insulina
In condizioni fisiologiche, l’insulina secreta dalle cellule β pancreatiche si lega al proprio recettore presente sulla membrana cellulare e attiva una cascata di segnalazione intracellulare. Questa via coinvolge diverse proteine, tra cui IRS-1, PI3K e Akt, che svolgono un ruolo fondamentale nella regolazione del metabolismo del glucosio.
Nei tessuti insulino-sensibili, in particolare nel muscolo scheletrico e nel tessuto adiposo, questa cascata di segnalazione promuove la traslocazione dei trasportatori del glucosio GLUT-4 dalle vescicole intracellulari alla membrana plasmatica. Una volta esposti sulla superficie cellulare, questi trasportatori consentono al glucosio presente nel sangue di entrare nella cellula, dove può essere utilizzato per produrre energia oppure immagazzinato sotto forma di glicogeno (Chadt & Al-Hasani, 2020; Huang et al., 2018).
Cosa accade quando si sviluppa insulino-resistenza
Quando si instaura una condizione di insulino-resistenza, la risposta biologica all’insulina si riduce e la captazione di glucosio mediata da GLUT-4 diventa meno efficiente. Questo significa che, a parità di concentrazione di insulina, i tessuti periferici utilizzano meno glucosio.
Nelle fasi iniziali questo fenomeno non comporta necessariamente un aumento della glicemia. L’organismo, infatti, tende a compensare la ridotta sensibilità all’insulina aumentando la secrezione pancreatica dell’ormone. Questa fase prende il nome di iperinsulinemia compensatoria e può mantenere i livelli di glicemia nei range di normalità anche per molti anni (Chadt & Al-Hasani, 2020).
Con il tempo, tuttavia, questa compensazione può diventare insufficiente, favorendo lo sviluppo di alterazioni metaboliche più evidenti.
Il ruolo dei trasportatori del glucosio nei diversi tessuti
I trasportatori GLUT-4 sono espressi soprattutto nel muscolo scheletrico e nel tessuto adiposo, dove rappresentano il principale meccanismo attraverso cui l’insulina stimola l’ingresso del glucosio nelle cellule.
Il fegato utilizza invece prevalentemente il trasportatore GLUT-2, caratterizzato da un’elevata capacità di trasporto e da una minore dipendenza dall’insulina per il semplice passaggio del glucosio nella cellula. In questo organo l’insulina svolge soprattutto un ruolo regolatorio sul metabolismo del glucosio, modulando processi come la glicogenosintesi, la glicogenolisi e la gluconeogenesi, contribuendo a ridurre la produzione endogena di glucosio nel periodo successivo al pasto (Hatting et al., 2018).
I meccanismi cellulari alla base dell’insulino-resistenza
L’insulino-resistenza non dipende esclusivamente da un difetto del recettore insulinico. Nella maggior parte dei casi è il risultato di alterazioni più complesse che coinvolgono la cascata di segnalazione intracellulare e il metabolismo energetico dei tessuti.
Tra i principali fattori associati allo sviluppo di insulino-resistenza figurano l’accumulo di lipidi intracellulari, la cosiddetta lipotossicità, l’infiammazione cronica di basso grado e lo stress ossidativo. Questi fenomeni possono interferire con la trasduzione del segnale insulinico e ridurre l’efficienza dei meccanismi che regolano la captazione del glucosio nei tessuti periferici (Fazakerley et al., 2019).
Sintomi e manifestazioni cliniche
Dal punto di vista clinico, l’insulino-resistenza è spesso asintomatica, soprattutto nelle fasi iniziali. Alcune persone riferiscono sintomi aspecifici come stanchezza, sonnolenza dopo pasti ricchi di carboidrati o maggiore senso di fame nelle ore successive al pasto.
Tuttavia questi segnali non sono né costanti né diagnostici. Per questo motivo l’insulino-resistenza viene generalmente identificata attraverso esami metabolici specifici e valutazioni cliniche più approfondite, piuttosto che sulla base della sola sintomatologia soggettiva (Chadt & Al-Hasani, 2020).
Fattori di rischio: sedentarietà e adiposità viscerale
L’insulino-resistenza è osservata più frequentemente in soggetti sedentari, con sovrappeso o con elevata adiposità viscerale. In queste condizioni il tessuto adiposo può diventare metabolicamente disfunzionale e aumentare il rilascio di acidi grassi liberi e mediatori infiammatori.
Questi fattori contribuiscono a interferire con la segnalazione insulinica e a peggiorare la sensibilità all’insulina nei diversi tessuti metabolici (Zhao et al., 2023).
Carboidrati, zuccheri e insulino-resistenza: un equivoco comune
Nella divulgazione nutrizionale è molto diffusa l’idea che l’insulino-resistenza e il diabete di tipo 2 siano direttamente causati dal consumo di carboidrati o di zuccheri semplici. In realtà questa interpretazione è concettualmente riduttiva e non riflette adeguatamente le evidenze fisiopatologiche disponibili.
La letteratura scientifica mostra infatti che uno dei principali determinanti dello sviluppo di insulino-resistenza è rappresentato da un bilancio energetico positivo cronico, soprattutto quando questo conduce ad un aumento della massa grassa e, in particolare, dell’adiposità viscerale. L’espansione del tessuto adiposo e l’accumulo di lipidi ectopici in organi come fegato e muscolo sono associati a lipotossicità, infiammazione cronica di basso grado e alterazioni della segnalazione insulinica (Samuel & Shulman, 2016; Czech, 2017).
In questo contesto anche la sedentarietà svolge un ruolo importante, poiché riduce la capacità del muscolo scheletrico di ossidare i substrati energetici e di utilizzare il glucosio, contribuendo al peggioramento della sensibilità insulinica.
Questo non significa che la composizione della dieta sia irrilevante. Pattern alimentari caratterizzati da un’elevata densità energetica e da un consumo frequente di alimenti altamente processati, spesso ricchi sia di zuccheri sia di grassi, possono facilitare l’aumento dell’introito calorico giornaliero e favorire nel tempo l’accumulo di massa grassa. In questo senso tali abitudini alimentari possono contribuire indirettamente allo sviluppo di insulino-resistenza, promuovendo un surplus energetico cronico e un peggioramento complessivo dello stato metabolico (Hall et al., 2019).
L’indice glicemico e il controllo del peso corporeo
Un altro concetto spesso frainteso riguarda l’utilizzo dell’indice glicemico (IG) degli alimenti per stabilire se un alimento “faccia ingrassare o dimagrire”. L’indice glicemico misura la velocità con cui un alimento contenente carboidrati aumenta la glicemia rispetto a un alimento di riferimento, ma non fornisce indicazioni dirette sull’impatto di quell’alimento sul peso corporeo.
La variazione del peso corporeo dipende principalmente dal bilancio energetico complessivo, cioè dal rapporto tra energia introdotta con la dieta ed energia consumata dall’organismo. Per questo motivo l’effetto di un singolo alimento sul peso non può essere interpretato indipendentemente dal contesto calorico generale della dieta.
Le evidenze scientifiche mostrano che diete a basso indice glicemico possono avere alcuni benefici metabolici in specifici contesti clinici, come nel controllo glicemico dei soggetti con diabete. Tuttavia, quando l’apporto calorico totale è comparabile, le differenze nell’indice glicemico della dieta hanno effetti relativamente modesti sulla perdita di peso (Livesey et al., 2008; Sacks et al., 2009).
Surplus calorico e sensibilità insulinica negli sportivi
Una riduzione della sensibilità insulinica può manifestarsi, almeno in parte, anche in soggetti fisicamente attivi quando vengono esposti per periodi prolungati a surplus energetici molto elevati, soprattutto se accompagnati da un aumento significativo della massa grassa.
Studi sperimentali di overfeeding hanno mostrato che periodi relativamente brevi di eccesso calorico possono ridurre la sensibilità insulinica, in particolare quando si osserva un aumento dell’accumulo di grasso corporeo (Walhin et al., 2013; Johannsen et al., 2014).
Nel contesto sportivo questo aspetto è rilevante perché una gestione poco controllata della fase di surplus calorico può tradursi in un peggiore partizionamento dei nutrienti, cioè una quota maggiore dell’energia introdotta che viene immagazzinata come tessuto adiposo anziché sostenere gli adattamenti muscolari e la performance (Slater et al., 2019).
Perché la letteratura suggerisce surplus calorici moderati
Per questo motivo, nella nutrizione sportiva applicata la letteratura tende a suggerire strategie di surplus energetico moderato e progressivo, piuttosto che aumenti calorici marcati e prolungati.
Le review dedicate alla fase off-season dei bodybuilder natural suggeriscono surplus generalmente nell’ordine del 10–20% del fabbisogno energetico, con l’obiettivo di favorire l’aumento della massa muscolare limitando l’accumulo eccessivo di massa grassa (Iraki et al., 2019).
Periodizzazione energetica: diet break e mini-cut
In questo contesto si inserisce il concetto di periodizzazione dell’introito energetico, con fasi di surplus controllato alternate, quando necessario, a brevi periodi di normocalorica o lieve deficit energetico.
Nella pratica questo approccio viene spesso tradotto in strategie come diet break o mini-cut. Le evidenze più solide riguardano soprattutto l’utilizzo di pause dalla dieta durante fasi ipocaloriche, dove possono contribuire a migliorare l’aderenza alla dieta e a preservare la massa magra.
Le prove dirette che dimostrino che i mini-cut durante una fase di surplus servano specificamente a preservare la sensibilità insulinica sono invece ancora limitate; il loro utilizzo si basa quindi soprattutto sull’obiettivo di contenere l’accumulo di massa grassa e mantenere una composizione corporea favorevole nel lungo periodo (Campbell et al., 2020).
Il ruolo dell’esercizio fisico nella sensibilità insulinica
L’esercizio fisico rappresenta uno dei più potenti strumenti per migliorare la sensibilità insulinica. L’attività muscolare aumenta infatti la captazione di glucosio nel muscolo non solo attraverso la via mediata dall’insulina, ma anche tramite meccanismi insulino-indipendenti legati alla contrazione muscolare e all’aumento della richiesta energetica.
Durante l’esercizio la contrazione muscolare stimola la traslocazione dei trasportatori GLUT-4 verso la membrana cellulare anche in assenza di insulina.
Tra i meccanismi coinvolti riveste un ruolo importante l’attivazione dell’enzima AMPK, sensibile allo stato energetico cellulare, che favorisce l’utilizzo del glucosio e degli acidi grassi come substrati energetici durante e dopo l’attività fisica (O’Neill, 2013; Richter & Hargreaves, 2013).
Conclusioni
L’insulino-resistenza rappresenta un fenomeno metabolico complesso che coinvolge diversi tessuti e molteplici meccanismi cellulari. Nelle fasi iniziali può rimanere clinicamente silente per lungo tempo grazie alla compensazione da parte del pancreas attraverso un aumento della secrezione insulinica.
Tra i fattori maggiormente associati allo sviluppo di insulino-resistenza figurano la sedentarietà, l’eccesso di adiposità viscerale e l’accumulo di lipidi ectopici, tutti elementi che interferiscono con la corretta segnalazione insulinica.
Nel contesto della nutrizione sportiva e della composizione corporea, la gestione dell’introito energetico assume un ruolo particolarmente rilevante. Surplus calorici eccessivi e prolungati possono favorire un aumento della massa grassa e contribuire a peggiorare la sensibilità insulinica, mentre strategie più moderate e progressivamente strutturate tendono a promuovere una migliore qualità degli adattamenti metabolici e muscolari.
Allo stesso tempo, l’attività fisica rimane uno dei fattori più efficaci per migliorare la sensibilità insulinica, grazie alla sua capacità di aumentare l’utilizzo del glucosio nei tessuti periferici attraverso meccanismi sia dipendenti sia indipendenti dall’insulina.
In sintesi, mantenere uno stile di vita attivo, controllare l’accumulo di massa grassa e adottare strategie nutrizionali sostenibili nel lungo periodo rappresentano elementi fondamentali per preservare una buona sensibilità insulinica e una salute metabolica ottimale.
Bibliografia
Chadt A., Al-Hasani H. (2020). Glucose transporters in adipose tissue, liver, and skeletal muscle in metabolic health and disease. Pflügers Archiv.
Huang X. et al. (2018). The PI3K/AKT pathway in obesity and type 2 diabetes. International Journal of Biological Sciences.
Hatting M. et al. (2018). Insulin regulation of gluconeogenesis. Annals of the New York Academy of Sciences.
Fazakerley D.J. et al. (2019). Muscle and adipose tissue insulin resistance. Journal of Lipid Research.
Zhao X. et al. (2023). The crucial role of insulin resistance in metabolic disease. Frontiers in Endocrinology.
Samuel V.T., Shulman G.I. (2016). The pathogenesis of insulin resistance. Cell.
Czech M.P. (2017). Insulin action and resistance in obesity and type 2 diabetes. Nature Medicine.
Hall K.D. et al. (2019). Ultra-processed diets cause excess calorie intake and weight gain. Cell Metabolism.
Livesey G. et al. (2008). Low glycaemic index diets and body weight: systematic review and meta-analysis. Obesity Reviews.
Sacks F.M. et al. (2009). Comparison of weight-loss diets with different compositions of fat, protein, and carbohydrates. New England Journal of Medicine.
Walhin J.P. et al. (2013). Exercise counteracts the effects of short-term overfeeding and reduced physical activity. The Journal of Physiology.
Johannsen D.L. et al. (2014). Effects of overfeeding on ectopic fat deposition and insulin sensitivity. Diabetes Care.
Slater G. et al. (2019). Is an energy surplus required to maximize skeletal muscle hypertrophy associated with resistance training? Frontiers in Nutrition.
Iraki J. et al. (2019). Nutrition recommendations for bodybuilders in the off-season. Sports.
Campbell B. et al. (2020). Intermittent energy restriction attenuates the loss of fat free mass. Journal of Functional Morphology and Kinesiology.
O’Neill H.M. (2013). AMPK and exercise: glucose uptake and insulin sensitivity. Diabetes & Metabolism Journal.
Richter E.A., Hargreaves M. (2013). Exercise, GLUT4, and skeletal muscle glucose uptake. Physiological Reviews.
Contatti
Per informazioni sui servizi o per richiedere una call conoscitiva gratuita, puoi contattarmi direttamente tramite email o WhatsApp. Risponderò personalmente per concordare modalità e obiettivi
© 2025. All rights reserved.
Visite Nutrizionali presso
Studi Medici NovaMedicea
via Aurelia Nord 304, Viareggio (LU)
Per prenotare una visita in ambulatorio è possibile contattare direttamente la struttura al numero: